LAG-3:雙抗療法的黃金搭檔
Novoprotein 2023-02-10 17:05 發表於上海
2022年8月22日,中國國家藥品監督管理局藥品評審中心(CDE)公示,中山康方生物醫藥有限公司「AK129注射液」的臨床試驗申請已獲得受理(受理號:CXSL2200395)。AK129注射是一種針對PD-1/LAG-3的特異性雙抗,不僅具有優越的抗原結合性,有效阻斷PD-1/LAG-3訊號通路,還可促進PBMC中IL-2和IFN-γ產生。在動物試驗中顯示出充分的抗腫瘤活性,且優於Relatlimab,顯示出廣泛的臨床前景[1]。

圖1. 來自CDE
LAG-3的分子特徵與結構
1990年,Triebel和他的同事透過篩選分離出在F5細胞(一種CD3陰性IL-2依賴性NK細胞系)中選擇性表達的分子,被確認為LAG-3。LAG-3是一種I型跨膜蛋白,它有四個Ig-like結構域,稱為結構域1(D1)到結構域4(D4)。LAG-3的胞外區域與CD4的胺基酸同源性約為20%,同樣由4個Ig-like結構域組成,細胞內區域沒有明顯的相似性。LAG-3缺乏與淋巴細胞特異性蛋白酪氨酸激酶(Lck)關聯所需的半胱氨酸基序和在CD4中觀察到的棕櫚醯化位點。CD4和LAG-3包含編碼細胞外區域的外顯子的基因組區域的組織是相似的,但包含編碼細胞內區域的外顯子的基因組區域的組織是不同的。因此,CD4和LAG-3密切相關,但卻表現出不同的功能[2-3]。
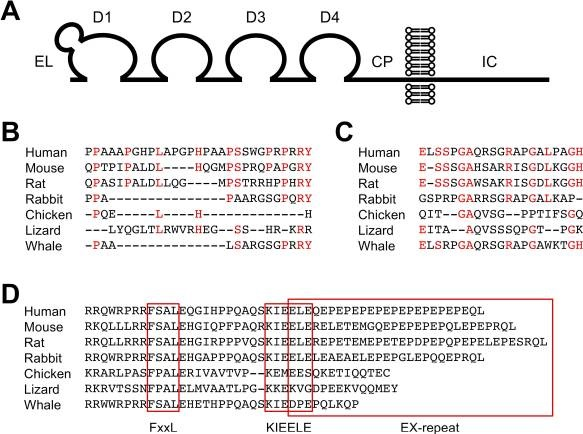
圖2. LAG-3結構與不同種屬間胺基酸比較結果[2]
LAG-3配體
在第一次發現LAG-3基因結構和CD4之間的相似性後,研究者對主要組織相容性複合體II (MHC-II)作為潛在配體進行了研究。表達LAG-3的COS-7細胞與攜帶MHC-II的B淋巴細胞結合,可以被anti-LAG-3 (clone 17B4)或anti-pan-HLA-II (clone D1.12) 阻斷。到目前為止,除了pMHCII外,還有幾種分子被報告為LAG-3的可能配體,Galectin-3和LSECtin已被證明與LAG-3上的聚醣相互作用。LSECtin是C型凝集素家族的成員,主要在肝臟表現。2019年,Wang等人發現纖維蛋白原家族的纖維蛋白原樣蛋白1 (FGL1)是LAG-3的潛在配體[4-5]。
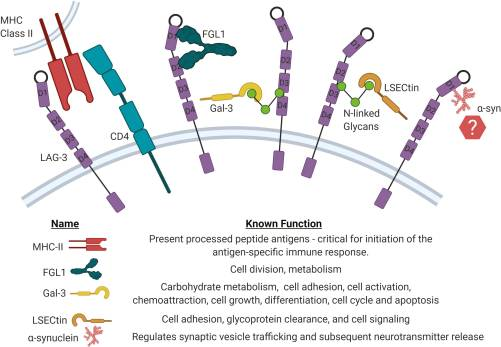
圖3. LAG-3潛在配體及其功能[4]
LAG-3在腫瘤中的表達
異常的LAG-3在人類腫瘤中廣泛存在,如黑色素瘤、非小細胞肺癌、大腸直腸癌、乳癌、肝細胞癌、濾泡性淋巴瘤、頭頸部鱗狀細胞癌等,與腫瘤的侵襲性進展和臨床病理特徵有顯著相關[6]。
表1. LAG-3在不同腫瘤中的表現及其臨床病理關係[6]
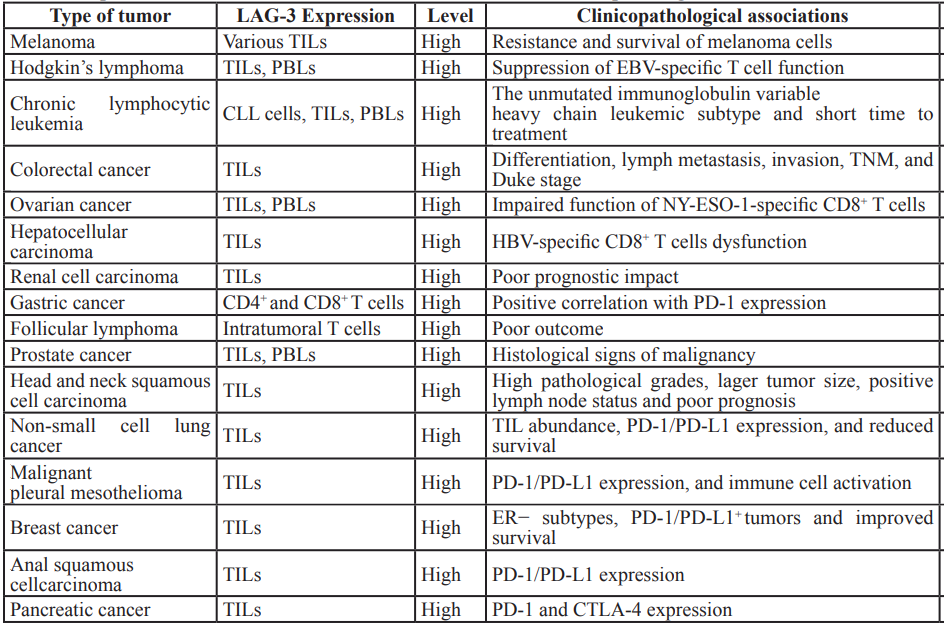
LAG-3與其他免疫檢查點之間相互作用
LAG-3與其他免疫檢查點有顯著的交互作用,尤其是PD-1。在T細胞聯合訊號通路中,TCR與MHC結合觸發T細胞啟動,而LAG-3等抑制免疫檢查點導致協同抑制TCR訊號[6 ]。
PD-1/PD-L1
越來越多的證據表明,LAG-3與典型的抑制性免疫檢查點PD-1/PD-L1聯用,可以共同介導免疫穩態,消除自體免疫疾病,增強腫瘤誘導的耐受性。PD-1和LAG-3已被報告廣泛共表達於CD4+,CD8+T細胞,特別是腫瘤浸潤T細胞。在小鼠黑色素瘤、纖維肉瘤和結直腸腺癌模型中已經報告了LAG-3和PD-1之間的顯著協同作用,對LAG-3和PD-1的聯合阻斷有效地根除了大多數已建立的腫瘤,這些腫瘤在很大程度上對單一藥物治療有抗藥性。雙基因敲除LAG-3和PD-1可延緩腫瘤生長,使小鼠壽命顯著延長。同樣,在小鼠卵巢癌模型中,LAG-3和PD-1協同抑制CD8+ T細胞效應功能。在許多患者的腫瘤樣本中,持續LAG-3和PD-1共同表現可調節T細胞耗竭狀態。例如,在NY-ESO-1卵巢癌樣本中,LAG-3和PD-1協同標記功能失調的CD8+ T細胞,兩者都會衰減活化CD8+T細胞,抑制細胞激素分泌,參與腫瘤細胞的免疫逃脫。最近在人類NSCLC中發現,TILs上LAG-3過度表現與PD-1/PD-L1表現有顯著相關,LAG-3和PD-L1均低表現的患者預後良好。總之,這些有價值的臨床前數據表明LAG-3和PD-1之間存在明顯的協同作用,為聯合治療策略提供了基礎。目前,大多數臨床試驗正在進行中,以探索同時靶向LAG-3和PD-1治療的好處[6]。點擊查看:PD-1、PD-L1相關產品。
CTLA-4
LAG-3調控的抗腫瘤免疫反應與CTLA-4相似,CTLA-4和LAG-3皆可抑制TCR訊號通路,阻斷細胞週期進程,負向調節T細胞穩態,觸發Tregs的免疫抑制功能,對DCs發揮重要作用。然而,LAG-3在抑制原代T細胞活化和記憶T細胞擴增方面可能更重要。它們訊號傳導路徑的現有交叉可能導致LAG-3和CTLA-4在功能上的相似性。二者均可透過共同抑制訊號路徑參與免疫耐受性。例如,在ACAID小鼠模型中,LAG-3和CTLA-4在CD4+ CD25+ Foxp3+ Tregs細胞上顯著上調,誘導了ACAID的發生。此外,pDCs誘導CD8 + Foxp3+ Treg細胞共表達LAG-3和CTLA-4,透過依賴CTLA-4的機制抑制異體反應性T細胞。在急性移植物抗宿主疾病(GVHD)中,人類和小鼠的實驗證據表明,使用四價CTLA-4-Ig和LAG-3-Ig共同阻斷可以協同抑制T細胞反應,預防急性GVHD,並降低GVHD死亡率。最近一項評估CTLA-4抗體ipilimumab治療效果的研究發現,在轉移性黑色素瘤患者中,ipilimumab可能增加表達LAG-3的腫瘤浸潤T細胞的頻率。此外,值得注意的是,最近開展了一項新的I/II期臨床試驗(NCT03459222),研究三靶點LAG-3、PD-1和CTLA-4的療效,這可能是治療癌症和自體免疫性疾病的一種新的組合策略[6]。點擊查看:CTLA-4相關產品。
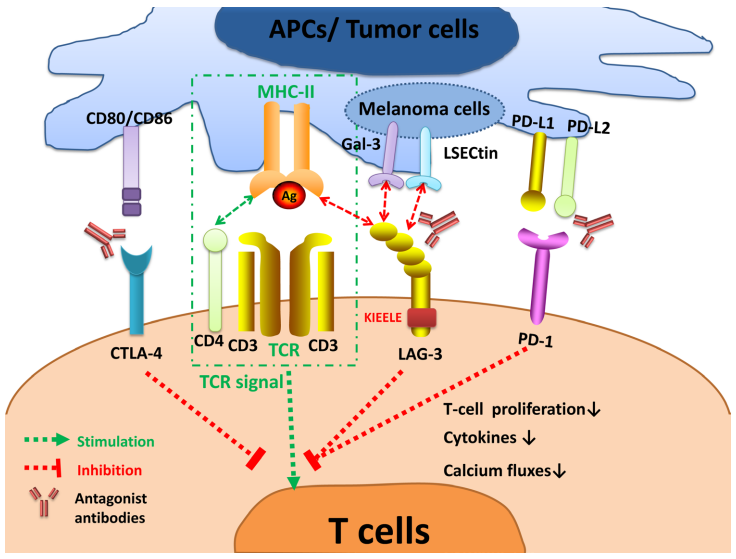
圖4. LAG-3信號以及與其他免疫檢查點的相互作用[6]
靶向LAG-3藥物研發進展
臨床前研究和初步臨床試驗表明LAG-3參與免疫抑制和抗腫瘤免疫。在過去的5年裡,針對LAG-3的藥物被開發出來用於治療癌症患者。目前至少有21種針對LAG-3的藥物在各種類型的癌症中進行臨床試驗。這些藥物可分為三種:抗LAG-3單克隆抗體,sLAG-3以及靶向LAG-3和 PD-1 / PD-L1 / CTLA-4的雙特異性抗體[7]。
表2. 靶點LAG-3的藥物臨床進展[7]
.png)
Novoprotein現貨供應LAG-3、PD-1、PD-L1、CTLA-4等靶點蛋白,可滿足單抗和雙抗等靶向藥物研發、功能評估及品質控制等不同環節的需求。
經過BLI驗證LAG-3與LAG-3抗體/ FGL-1配體均具有高親和力
.png)
Loaded Anti-Human LAG-3 mAb-Fc(Cat#NC067) on Protein A Biosensor, can bind Human LAG-3-6His(Cat#CU29) with an affinity constant of 0.41 nM as determined in BLI assay.
%20on%20Protein.png)
Loaded Human FGL1-Fc(Cat#CW68) on Protein A Biosensor, can bind Human LAG-3-His(Cat#CU29) with an affinity constant of 88.12 nM as determined in BLI assay.
| Cat. No. | Product Name |
| CJ91 | Recombinant Human LAG-3 (Leu23-Gly434,C-6His) |
| CU29 | Recombinant Human LAG-3 (Leu23-Leu450,C-6His) |
| CU30 | Recombinant Human LAG-3 (C-Fc) |
| CW44 | Recombinant Human LAG-3 (C-mFc) |
| CY12 | Biotinylated Human LAG-3 (C-6His-Avi) |
| CK56 | Recombinant Mouse LAG-3 (C-6His) |
| C998 | Recombinant Cynomolgus LAG-3 (N-8His) |
| CP99 | Recombinant Cynomolgus LAG-3 (C-Fc) |
| NC067 | Anti-Human LAG-3 mAb |
| C068 | Recombinant Human Galectin-3 (Tag free) |
| C846 | Recombinant Human Galectin-3 (C-6His) |
| CW55 | Recombinant Human FGL1 (C-6His) |
| CW62 | Recombinant Human FGL1 (C-mFc) |
| CW68 | Recombinant Human FGL1 (C-Fc) |
| CY21 | Biotinylated Human FGL1 (C-Avi-6His) |
| CY19 | Biotinylated Human FGL1 (C-Fc-Avi) |
| CW69 | Recombinant Cynomolgus FGL1 (C-6His) |
| CY20 | Biotinylated Cynomolgus FGL1 (C-Avi-6His) |
參考文獻
[1]. 康方生物官網;
[2]. Maruhashi T, Sugiura D, Okazaki IM, Okazaki T. LAG-3: from molecular functions to clinical applications. J Immunother Cancer. 2020 Sep;8(2):e001014. doi: 10.1136/jitc-2020-001014. PMID: 32929051; PMCID: PMC7488795.
3]. Lecocq, Quentin et al. “The Next-Generation Immune Checkpoint LAG-3 and Its Therapeutic Potential in Oncology: Third Time's a Charm.” International journal of molecular sciences vol. 22,1 75. 23 Dec. 2020, doi:10.3390/ijms22010075.
[4]. Burnell SEA, Capitani L, MacLachlan BJ, Mason GH, Gallimore AM, Godkin A. Seven mysteries of LAG-3: a multi-faceted immune receptor of increasing complexity. Immunother Adv. 2021 Dec 20;2(1):ltab025. doi: 10.1093/immadv/ltab025. PMID: 35265944; PMCID: PMC8895726.
[5]. Wang J, Sanmamed MF, Datar I, et al. Fibrinogen-Like protein 1 is a major immune inhibitory ligand of LAG-3. Cell 2019;176:334–47. 10.1016/j.cell.2018.11.010.
[6]. Long, Long et al. “The promising immune checkpoint LAG-3: from tumor microenvironment to cancer immunotherapy.” Genes & cancer vol. 9,5-6 (2018): 176-189. doi:10.18632/genesandcancer.180.
[7]. Zhao, Lishu et al. “Update on lymphocyte-activation gene 3 (LAG-3) in cancers: from biological properties to clinical applications.” Chinese medical journal vol. 135,10 1203-1212. 20 May. 2022, doi:10.1097/CM9.0000000000001981.
